Introduction
L'électrodéposition est untechnique électrochimiqueavec une histoire qui s'étend sur plus de deux siècles et qui implique le dépôt de matériaux sur une surface conductrice par l'application de courant électrique. Depuis sa création-depuis la première pile voltaïque de Volta en 1800 jusqu'à la découverte par Davy du sodium et du potassium par électrolyse en 1807, l'électrodéposition est devenue uneprocessus sophistiquéessentiel dans diverses applications industrielles et de recherche. Cette méthode polyvalente est désormais utilisée dans des domaines allant deélectronique et conversion d'énergieà la protection contre la corrosion et à la synthèse de matériaux catalytiques. L'attrait fondamental de l'électrodéposition réside dans sa capacité à contrôler avec précision l'épaisseur, la composition et la structure des matériaux déposés, souvent à des températures relativement basses et avec des coûts d'équipement minimes par rapport aux techniques de dépôt sous vide-.
Cet article fournit un aperçu complet de l'électrodéposition, couvrant sesprincipes de base, le différentapproches technologiques, et leméthodes de caractérisationutilisé pour analyser les matériaux électrodéposés. Que vous soyez nouveau dans le domaine ou que vous cherchiez à approfondir vos connaissances, ce guide éclairera la science derrière cette puissante technique de traitement des matériaux.

1 Principes fondamentaux de l'électrodéposition
1.1 Concepts de base et contexte historique
L'électrodéposition est unprocessus électrochimiqueoù les ions métalliques en solution sont réduits sur un substrat conducteur sous l'influence d'un champ électrique externe. Ce processus se produit à travers lemigration d'ionsdans une solution électrolytique vers des électrodes de charge opposée, où elles subissent des réactions d'oxydation ou de réduction.
L’importance historique de l’électrodéposition ne peut être surestimée. La technique a joué un rôle déterminant dans les découvertes scientifiques fondamentales et les applications industrielles. Son développement sur plus dedeux cents ansl'a transformé d'une curiosité de laboratoire en un processus industriel indispensable utilisé dans le monde entier pour la synthèse des matériaux et l'ingénierie des surfaces.
1.2 Principe de fonctionnement
À la base, l’électrodéposition repose surLes lois de Faraday sur l'électrolyse, qui établissent une relation quantitative entre la quantité de charge électrique traversant un électrolyte et la masse de matériau déposée au niveau des électrodes. La première loi stipule que la masse de substance déposée sur une électrode est directement proportionnelle à la quantité d’électricité traversant le circuit. La deuxième loi stipule que les masses des différentes substances libérées par la même quantité d'électricité sont proportionnelles à leurs poids équivalents.
Le processus d'électrodéposition se déroule généralement dans uncellule électrochimiquecontenant une solution électrolytique avec des sels métalliques dissous. Lorsqu'un potentiel externe est appliqué entre deux électrodes, les cations métalliques (ions chargés positivement) migrent vers la cathode (électrode négative), où ils gagnent des électrons et sont réduits pour former une couche métallique solide :

OùMn+est un ion métallique avec n charges positives, etMest l’atome de métal neutre incorporé dans le dépôt en croissance.
Simultanément, au niveau de l'anode (électrode positive), soit une oxydation des atomes métalliques se produit (dans le cas des anodes solubles) libérant des ions métalliques dans la solution, soit un dégagement d'oxygène se produit (dans le cas des anodes inertes).
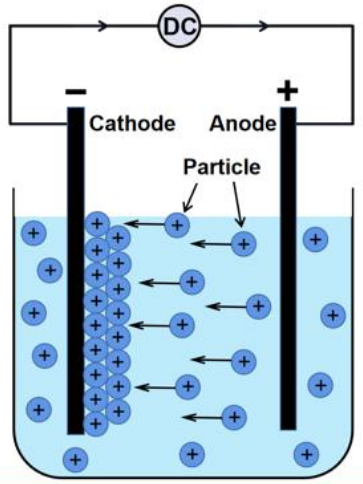
Tableau : Principaux composants de l'électrodéposition
| Composant | Fonction | Exemples |
|---|---|---|
| Anode | Source d'ions métalliques ou site de dégagement d'oxygène | Cuivre, nickel, platine (inerte) |
| Cathode | Surface où se produit le dépôt | Substrats conducteurs (métaux, semi-conducteurs) |
| Électrolyte | Contient des ions métalliques et permet la conduction ionique | Solutions aqueuses de sels métalliques |
| Alimentation | Fournit de l’énergie électrique pour le processus | Source d'alimentation CC, potentiostat/galvanostat |
1.3 Configuration des électrodes : systèmes à deux-électrodes ou à trois-électrodes
Les systèmes d'électrodéposition sont généralement configurés en utilisant soitdeux-électrodesoutrois-électrodesconfigurations.
Lesystème à deux-électrodesse compose d’une électrode positive (anode) et d’une électrode négative (cathode), toutes deux immergées dans l’électrolyte. L'alimentation électrique ou le poste de travail électrochimique fournit une tension entre ces deux électrodes. Dans cette configuration, la tension mesurée représente latension totale des cellulesdans toute la cellule électrochimique.
Lesystème à trois-électrodesest plus avancé et comprend :
1. Électrode de travail (NOUS): Il s'agit de l'électrode où se produit la réaction électrochimique d'intérêt (dépôt). Il sert de substrat pour le dépôt de matériaux.
2. Contre-électrode (CE): Également appelée électrode auxiliaire, elle complète le circuit électrique et permet au courant de circuler dans la cellule. Il est généralement constitué de matériaux inertes comme le platine ou le graphite.
3. Électrode de référence (RE): Cette électrode maintient un potentiel stable et connu par rapport auquel le potentiel de l'électrode de travail peut être mesuré et contrôlé avec précision. Les électrodes de référence courantes comprennent l'électrode au calomel saturé (SCE), l'électrode Ag/AgCl et l'électrode Hg/HgO.
Dans le système à trois -électrodes, l'électrode de référence est positionnée à proximité de l'électrode de travail pour minimiser les erreurs dues à la résistance de la solution (chute IR) et aux fluctuations de tension. Cette disposition permetcontrôle précisdu potentiel de l'électrode de travail, ce qui le rend idéal pour les applications de recherche où la précision est essentielle.
La configuration à trois -électrodes est particulièrement intéressante, car elle permet aux chercheurs de contrôler avec précision le potentiel au niveau de l'électrode de travail sans interférence due aux pertes ohmiques ou aux modifications au niveau de la contre-électrode. Cette précision est essentielle pour les études fondamentales des mécanismes de dépôt et pour produire des dépôts aux propriétés spécifiques.
2 techniques d'électrodéposition
Diverses méthodes d'électrodéposition ont été développées pour répondre aux différentes exigences en matière de matériaux et aux besoins d'application. Chaque technique offre des avantages uniques en termes de contrôle des propriétés des dépôts, d'efficacité du traitement et d'applicabilité à différents systèmes de matériaux.
2.1 Électrodéposition conventionnelle

Électrodéposition conventionnelleenglobe les méthodes de base à tension constante ou à courant constant qui constituent la base de la technologie de galvanoplastie. Cette approche consiste généralement à appliquer unecourant continu continu(DC) entre l'anode et la cathode, ce qui entraîne un taux de dépôt relativement constant tout au long du processus.
La simplicité de l'électrodéposition conventionnelle la rend largement applicable dans les environnements industriels pour des applications telles que les finitions décoratives, les revêtements résistants à la corrosion-et les interconnexions électroniques. Il offre cependantcontrôle limitésur la microstructure des dépôts et peut produire des dépôts avec une morphologie variable et une structure de grains relativement grossiers par rapport aux techniques plus avancées.
2.2 Électrodéposition galvanostatique (courant constant)

Électrodéposition galvanostatiquemaintient uncourant constantentre les électrodes de travail et les contre-électrodes pendant le processus de dépôt. La réponse enregistrée est le potentiel de la cellule électrochimique (dans un système à deux-électrodes) ou de l'électrode de travail (dans un système à trois-électrodes) en fonction du temps.
Contrairement au dépôt à potentiel constant, qui peut commencer immédiatement après l'application potentielle, le dépôt galvanostatique nécessite une brève période pour démarrer. En effet, une partie du courant appliqué doit d'abord charger lecapacité double couche(Cdl) à l'interface électrode-électrolyte. Lorsque le potentiel atteint un certain seuil (généralement le potentiel d’équilibre plus le surpotentiel), la réaction électrochimique commence.
Le courant constant (I) appliqué se compose de deux composants : Idl (le courant capacitif de charge Cdl) et Ict (le courant de transfert de charge pour l'électrodéposition). Lorsque le dépôt commence, Idl se rapproche rapidement de zéro. La courbe de potentiel-temps (courbe V-t) obtenue lors du dépôt galvanostatique contient des informations essentielles sur les processus électrochimiques se produisant lors du dépôt.
Le principal avantage du dépôt galvanostatique est sa capacité à maintenir unetaux de dépôt constant, ce qui est particulièrement utile pour les processus industriels où le contrôle de l'épaisseur est critique. Cependant, le potentiel peut varier au cours du dépôt, affectant potentiellement les propriétés du dépôt s'il n'est pas soigneusement contrôlé.
2.3 Électrodéposition potentiostatique (potentiel constant)

Électrodéposition potentiostatiqueconsiste à appliquer unpotentiel constantentre les électrodes positives et négatives (dans un système à deux-électrodes) ou entre les électrodes de travail et les contre-électrodes (dans un système à trois-électrodes). Le potentiel de dépôt est maintenu constant par le poste de travail électrochimique et le courant est enregistré en fonction du temps.
En fonction de la relation entre le potentiel appliqué et le potentiel d'équilibre thermodynamique, le dépôt potentiostatique peut être classé en deux régimes :
1. Dépôt sous potentiel (UPD): Cela se produit à des potentiels inférieurs au potentiel d’équilibre thermodynamique. L'UPD implique des processus d'adsorption, de nucléation et de croissance déterminés par les caractéristiques de surface du substrat (composition chimique, structure cristalline, morphologie et mouillabilité de l'électrolyte) et les interactions ioniques-substrat. Les types de cations et d'anions présents dans l'électrolyte influencent considérablement la structure, les propriétés et la cinétique de dépôt du matériau déposé.
2. Dépôt surpotentiel (OPD): Cela se produit à des potentiels supérieurs au potentiel d’équilibre thermodynamique. La structure et les propriétés de l'OPD dépendent fortement de divers facteurs, notamment le surpotentiel (la différence entre les potentiels appliqués et d'équilibre), la concentration en électrolyte, le mécanisme de croissance et les interactions entre les dépôts et le substrat. Notamment, la nucléation contrôlée par diffusion-est généralement l'étape-déterminante du taux pour l'OPD, tandis que l'incorporation du réseau dans le substrat est l'étape-déterminante du taux pour l'UPD.
Le principal avantage du dépôt potentiostatique estcontrôle précissur la force motrice du dépôt, ce qui permet une meilleure manipulation des processus de nucléation et de croissance. Cela aboutit souvent à des dépôts avec une morphologie plus uniforme et une structure de grain plus fine.
2.4 Co-électrodéposition
Co-électrodépositionest une technique utilisée pour préparermatériaux compositesoualliagesen déposant simultanément deux ou plusieurs éléments de la même solution électrolytique. Cette méthode est particulièrement utile pour créer des matériaux dotés de propriétés améliorées qui ne peuvent pas être obtenues avec des dépôts d'éléments uniques.
La co-électrodéposition permet la production de nanomatériaux hautement poreux avec des surfaces spécifiques élevées, qui sont précieux pour les applications nécessitant une activité électrocatalytique intrinsèque élevée. Le processus nécessite un contrôle minutieux de la composition de l'électrolyte, du pH, de la température et des paramètres de dépôt pour garantir un co-dépôt uniforme des différents éléments avec la composition et la structure souhaitées.
Cette technique est largement utilisée pour produire des dépôts d'alliages (tels que le laiton, le bronze ou le nickel-phosphore) et des composites à matrice métallique contenant des particules dispersées de céramiques, de polymères ou d'autres métaux.
2.5 Électrodéposition hydrothermale

Électrodéposition hydrothermalecombine le dépôt électrochimique avectempérature et pression élevéesconditions dans un réacteur autoclave. Cette méthode est particulièrement utile pour produire des électrocatalyseurs avechaute cristallinitéet des structures-bien définies.
L'environnement hydrothermal améliore la mobilité des ions et la cinétique de réaction, ce qui entraîne souvent des dépôts présentant une adhérence, une densité et une cristallinité améliorées par rapport à l'électrodéposition à température ambiante. La technique est particulièrement intéressante pour déposer des oxydes métalliques et d’autres composés bénéficiant de conditions de synthèse hydrothermales.
Les matériaux déposés par électrolyse hydrothermique présentent souvent une activité électrocatalytique améliorée en raison de leurs caractéristiques structurelles améliorées, ce qui les rend particulièrement adaptés aux applications de conversion d'énergie.
2.6 Électrodéposition assistée par micro-ondes-

Électrodéposition assistée par micro-ondes-utiliserayonnement micro-ondespour améliorer le processus de dépôt. Cette technique avancée peut produire des revêtements hautement mésoporeux avec des structures uniques qui contribuent à des performances électrocatalytiques efficaces.
Le champ micro-ondes interagit avec l’électrolyte et le dépôt croissant via plusieurs mécanismes :
Chauffage diélectriquede la solution, entraînant une augmentation rapide de la température
Effets non-thermiquessur les processus de migration ionique et de transfert de charge
Modification de la nucléation et de la croissancecinétique
Ces effets peuvent conduire à des taux de dépôt accélérés, à des structures de grains raffinées et à des caractéristiques morphologiques uniques difficilement réalisables par les méthodes d'électrodéposition conventionnelles. L'électrodéposition assistée par micro-ondes-est particulièrement utile pour créer des revêtements hautement poreux et à grande surface--pour les applications catalytiques et de stockage d'énergie.
Tableau : Comparaison des techniques d'électrodéposition
| Technique | Paramètre de contrôle clé | Principaux avantages | Applications typiques |
|---|---|---|---|
| Galvanostatique | Courant constant | Vitesse de dépôt maîtrisée, simplicité | Placage industriel, contrôle d'épaisseur |
| Potentiostatique | Potentiel constant | Contrôle de potentiel précis, morphologie uniforme | Recherche, matériaux nanostructurés |
| Co-dépôt | Plusieurs éléments | Matériaux composites, formation d'alliages | Revêtements fonctionnels, catalyseurs |
| Hydrothermale | Température/pression | Haute cristallinité, adhérence améliorée | Oxydes métalliques, matériaux énergétiques |
| Micro-ondes-assisté | Rayonnement micro-ondes | Structures mésoporeuses, morphologies uniques | Revêtements catalytiques, stockage d'énergie |
3 Techniques de caractérisation des matériaux électrodéposés
Une bonne caractérisation des matériaux électrodéposés est essentielle pour comprendre leurs propriétés et optimiser les paramètres de dépôt. Plusieurs techniques analytiques avancées sont couramment utilisées à cette fin.
3.1 Diffraction des rayons X- (DRX)

-Diffraction des rayons X (DRX)est une puissante technique non destructive-utilisée pour analyserstructure cristallinede matériaux électrodéposés. La XRD fonctionne en irradiant un échantillon avec des rayons X- et en mesurant les angles et les intensités des faisceaux diffractés qui émergent.
Lorsque les rayons X-interagissent avec un matériau cristallin, ils subissent une diffraction selonloi de Bragg:

Où λ est la longueur d'onde des rayons X-, d est l'espacement entre les plans atomiques, θ est l'angle de diffraction et n est un nombre entier.
XRD fournit des informations essentielles sur :
Structure cristallineet composition des phases
Orientation privilégiée(texture) des cristallites
Taille des cristallitesgrâce à l'analyse de l'élargissement du pic
Paramètres de réseauet tendre
Par exemple, lors de l'électrodéposition de films de Cu₂O sur du verre conducteur, l'analyse DRX a révélé que les films déposés à 60 degrés commençaient à développer une orientation préférée (111). À mesure que la température du bain augmentait, la taille des grains des films de Cu₂O augmentait de 0,2 μm à 0,4 μm, démontrant comment la DRX peut suivre les changements microstructuraux résultant de différents paramètres de dépôt.
La DRX est particulièrement utile pour identifier différentes phases dans les dépôts d'alliages ou les revêtements composites et pour surveiller les changements structurels qui se produisent lors des traitements post-dépôt tels que le recuit.
3.2 Microscopie électronique à balayage (MEB)

Microscopie électronique à balayage (MEB)est utilisé pour examiner lemorphologie de la surfaceetmicrostructurede matériaux électrodéposés à fort grossissement. SEM fonctionne en balayant un faisceau d'électrons focalisé sur la surface de l'échantillon et en détectant divers signaux générés par les interactions électron-matière.
Les principaux signaux utilisés pour l’imagerie en SEM comprennent :
Électrons secondaires (SE): Produit par des interactions inélastiques entre le faisceau d'électrons et les atomes de l'échantillon, fournissant un contraste topographique.
Électrons rétrodiffusés (ESB): Résultant de la diffusion élastique des électrons incidents, produisant un contraste de composition basé sur les différences de numéro atomique.
SEM fournit des informations détaillées sur :
Morphologie des surfaceset architecture de dépôt
Taille des grainset distribution
Porositéet structure des défauts
Morphologie transversale-et épaisseur du dépôt
Par exemple, la caractérisation SEM de films de Cu₂O électrodéposés a révélé unstructure de surface semblable à un réseau poreux-. Dans une autre étude, le SEM a été utilisé pour caractériser des réseaux de nanofils de cuivre préparés par électrodéposition pulsée dans des modèles d'oxyde d'aluminium anodique (AAO), montrant comment l'intensité de courant de pointe et les cathodes auxiliaires affectaient la qualité de surface et l'uniformité de la distribution de longueur.
Les systèmes SEM avancés peuvent inclurespectroscopie de rayons X-dispersive-d'énergie (EDS)capacités d’analyse élémentaire, permettant aux chercheurs de déterminer la composition chimique des matériaux électrodéposés à l’échelle microscopique8.
3.3 Spectroscopie photoélectronique à rayons X- (XPS)

Spectroscopie photoélectronique à rayons X- (XPS), également connue sous le nom de spectroscopie électronique pour l'analyse chimique (ESCA), est une technique sensible à la surface-qui fournit des informations sur lacomposition chimiqueetétat électroniqued'éléments en matériaux électrodéposés.
XPS fonctionne sur la base dueffet photoélectrique: lorsqu'un matériau est irradié avec des rayons X-, des électrons sont éjectés des coques internes des atomes. L'énergie cinétique de ces photoélectrons est mesurée et liée à leur énergie de liaison par l'équation :
![]()
Où KE est l'énergie cinétique de l'électron éjecté, hν est l'énergie du photon des rayons X-, BE est l'énergie de liaison de l'électron et φ est le travail de travail du spectromètre.
XPS fournit des informations précieuses sur :
Composition élémentairede la surface (généralement les 1 à 10 nm supérieurs)
État chimiquedes éléments (état d'oxydation, environnement chimique)
Uniformité de compositionà travers la surface
Épaisseurde couches de surface et de revêtements
Dans l'analyse des films de Cu₂O électrodéposés, XPS a confirmé lehaute puretédu matériau déposé, démontrant l'utilité de la technique pour vérifier la composition et la pureté du dépôt.
XPS est particulièrement utile pour analyser les films minces et les modifications de surface où l'état chimique des éléments à la surface influence fortement les propriétés des matériaux. Il peut détecter la contamination, les états d’oxydation et l’efficacité des traitements de surface.
Tableau : Techniques de caractérisation des matériaux électrodéposés
| Technique | Informations obtenues | Profondeur analysée | Considérations spéciales |
|---|---|---|---|
| DRX | Structure cristalline, composition des phases, taille des grains, texture | En vrac (μm en mm) | Nécessite un matériau cristallin |
| MEB | Morphologie de surface, microstructure, épaisseur | Surface/volume (nm en mm) | Peut nécessiter un revêtement conducteur |
| XPS | Composition élémentaire, état chimique, état d'oxydation | Surface (1-10 nm) | Ultra-vide poussé requis |
4 facteurs influençant l'électrodéposition
Plusieurs paramètres influencent de manière significative le processus d'électrodéposition et les propriétés des dépôts obtenus. Comprendre et contrôler ces facteurs est essentiel pour produire des matériaux présentant les caractéristiques souhaitées.
Densité de courant(courant par unité de surface) affecte directement le taux de dépôt et les propriétés du dépôt. Des densités de courant plus élevées augmentent généralement la vitesse de dépôt mais peuvent conduire à des dépôts rugueux et poreux avec une mauvaise adhérence s'ils sont excessivement élevés. Différents matériaux ont des plages de densité de courant optimales qui produisent des dépôts lisses et denses.
Lecomposition électrolytique, y compris la concentration en ions métalliques, le pH et la présence d'additifs, influencent de manière significative le comportement des dépôts. Des additifs tels que des azurants, des niveleurs et des -réducteurs de contrainte sont souvent utilisés pour modifier les propriétés des dépôts. La concentration d'ions métalliques affecte la densité de nucléation et le mode de croissance.
4.3 Température
Températureaffecte la mobilité des ions, les taux de diffusion et la cinétique de réaction. Des températures plus élevées augmentent généralement les taux de dépôt et peuvent améliorer l’adhérence et la densité des dépôts. Cependant, des températures trop élevées peuvent entraîner une rugosité accrue et une puissance de projection réduite (capacité à se déposer uniformément sur des surfaces irrégulières).
LepH de l'électrolyteinfluence la spéciation des ions métalliques et leurs potentiels de réduction. Cela peut affecter la stabilité des complexes dans la solution, la réaction de dégagement d’hydrogène (qui entre en compétition avec le dépôt de métal) et les propriétés du matériau déposé. Le maintien d’un pH approprié est crucial pour des résultats cohérents.
5 applications de l'électrodéposition
L'électrodéposition trouve des applications dans de nombreux domaines en raison de sa polyvalence et de sa-rentabilité :
L'une des applications les plus anciennes et les plus répandues de l'électrodéposition consiste à produirerevêtements décoratifs et protecteurs. Les revêtements de chrome, de nickel, de zinc et de métaux précieux sont largement utilisés dans les industries de l'automobile, de l'aérospatiale et des biens de consommation pour la protection contre la corrosion, la résistance à l'usure et l'esthétique.
Dans l’industrie électronique, l’électrodéposition est utilisée pour fabriquertraces conductrices, interconnexions, etvia des-vias en siliciumdans les dispositifs semi-conducteurs. L’électrodéposition du cuivre est particulièrement importante pour la fabrication de circuits intégrés en raison de son excellente conductivité électrique.
Les matériaux électrodéposés jouent un rôle crucial danstechnologies énergétiquescomme les batteries, les piles à combustible et les cellules solaires. La technique est utilisée pour produire des électrodes à grande surface, des matériaux catalytiques pour les piles à combustible et des films minces pour les dispositifs photovoltaïques.
L'électrodéposition peut produirenanostructures très poreusesavec de grandes surfaces, ce qui les rend idéaux pour les applications catalytiques. Des matériaux tels que des oxydes de métaux de transition et des métaux nobles peuvent être déposés en tant que catalyseurs efficaces pour diverses réactions chimiques, notamment les réactions de dégagement d'hydrogène, de dégagement d'oxygène et de réduction de l'oxygène.
Conclusion
L’électrodéposition est une technique polyvalente et puissante pour fabriquer des matériaux fonctionnels aux structures et propriétés contrôlées. De ses principes fondamentaux basés sur les réactions électrochimiques aux techniques avancées telles que le dépôt hydrothermal et assisté par micro-ondes-, le domaine propose de nombreuses approches pour la synthèse des matériaux.
Les techniques de caractérisation abordées-XRD, SEM et XPS-fournissent des outils essentiels pour comprendre les relations entre les paramètres de dépôt et les propriétés des matériaux résultants. Ces connaissances permettent la conception rationnelle de matériaux électrodéposés pour des applications spécifiques dans divers domaines, notamment l'électronique, l'énergie, la catalyse et l'ingénierie des surfaces.
À mesure que la recherche progresse, les techniques d'électrodéposition évolueront probablement pour permettre un contrôle encore plus poussé de la structure des matériaux à l'échelle nanométrique, ouvrant ainsi de nouvelles possibilités pour les matériaux et les dispositifs de la prochaine-génération. La combinaison d’une compréhension théorique, d’une expertise expérimentale et d’une caractérisation avancée fait de l’électrodéposition un outil indispensable dans la science et l’ingénierie des matériaux modernes.
